工學院熊春陽團隊與合作者發現抑製非肌肉肌球蛋白II活性可增強T細胞腫瘤殺傷效能
2025/02/09 信息來源: 工學院
編輯💆♂️:青苗 | 責編⛑:安寧腫瘤免疫療法從根本上重塑了腫瘤治療的格局,而T細胞是腫瘤免疫治療中的關鍵細胞,因此在治療過程確保T細胞的免疫活性成為成功治療的關鍵之一。
越來越多的研究表明✴️👜,機械力學因素和生化因素一樣影響T細胞的免疫活性👨🏭。研究團隊在前期的工作中發現,機械力敏感通道PIEZO1可以作為“生物力學免疫檢查點”調控T細胞抗腫瘤免疫功能🗄,阻斷PIEZO1會增強T細胞腫瘤殺傷效能(Nature Biomedical Engineering 2024, 8:1162—1176)👨🏽🏫。然而♗,機械力-生化信號轉導通路上其他分子是否也參與T細胞抗腫瘤免疫功能調控,仍然不清楚。
近日,工學院教授熊春陽團隊聯合中國醫學科學院基礎醫學研究所研究員劉玉英團隊在Science Advances發表了題為“Suppression of non-muscle myosin II boosts T cell cytotoxicity against tumors”的論文,發現抑製非肌肉肌球蛋白II(NM II)增加了T細胞的牽引力,進而增強了其對腫瘤細胞的細胞毒性📃,進一步解析了生物力學因素如何影響T細胞腫瘤殺傷效能。
通過使用來自小鼠和不同類型腫瘤患者的T細胞👞,研究團隊發現低劑量非肌肉肌球蛋白II的抑製劑Blebbistatin可以增強T細胞對腫瘤細胞的細胞毒性🎆👩🏿🎤,且不影響細胞因子的分泌以及顆粒酶B👨🏿🔬🧜🏼、穿孔素的產生;部分抑製非肌肉肌球蛋白II活性增強了CD8+T細胞的牽引力(牽引力顯微鏡測量結果),也提高了T細胞與腫瘤細胞間的粘附力(流體力顯微鏡測量結果)👩🏿🦰,提示非肌肉肌球蛋白II參與調控T細胞腫瘤殺傷效能(圖1)。
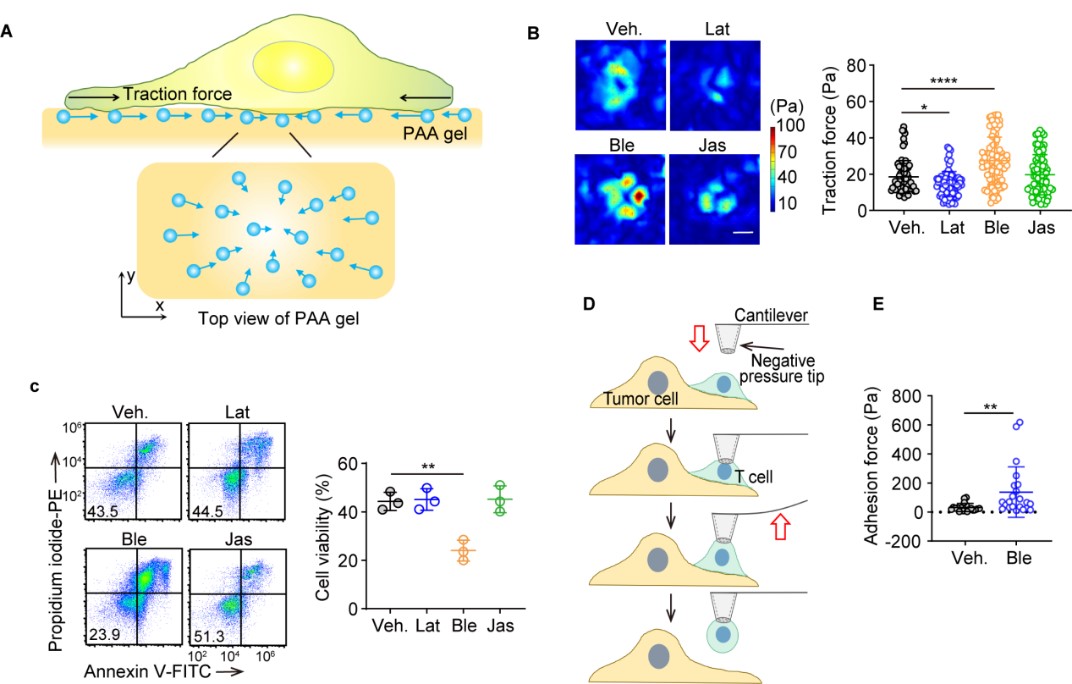
圖1. 抑製NM II增強T細胞牽引力及腫瘤殺傷效能。a)T細胞牽引力檢測示意圖🛟;b)小分子藥物抑製NM II增強T細胞牽引力;c)小分子藥物抑製NM II增強T細胞的腫瘤殺傷效果👩🦼➡️🧏🏽♂️;d)流體力顯微鏡檢測T細胞與腫瘤細胞間粘附力👨🦼;e)小分子藥物抑製NM II增強T細胞與腫瘤細胞間粘附
進一步探究其機理發現:非肌肉肌球蛋白II上調轉錄因子NKX3-2活性,進而增加其靶基因ADGRB3表達🤙🏻;而ADGRB3上調則抑製絲狀肌動蛋白(F-actin)動態重塑👱🏻,導致T細胞牽引力下降,最終減弱了T細胞腫瘤殺傷功能(圖2)💨。在動物腫瘤模型中↘️🖕🏿,靶向T細胞NMII-NKX3-2-ADGRB3通路能有效抑製腫瘤生長,延長生存期。在結直腸癌👴🏿、胃癌和肝癌等腫瘤病人樣本中,也發現NKX3-2、ADGRB3表達水平與患者CD8+T細胞的浸潤程度、免疫治療效果負相關。
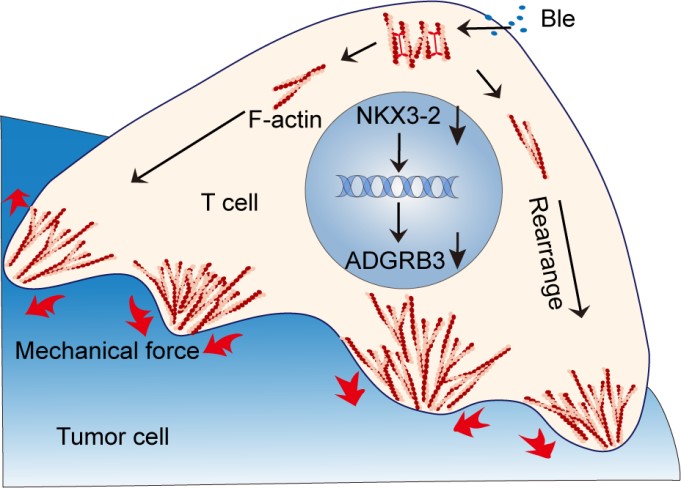
圖2. NMII-NKX3-2-ADGRB3信號通路調控T細胞腫瘤殺傷的力學生物學機製示意
該研究為機械力信號調控T細胞抗腫瘤免疫功能提供了新的證據,也為研發更有效的腫瘤免疫療法提供了生物力學新策略🍷🧑🏻🦯。
熊春陽、劉玉英🏮🚴🏽、李開龍教授為該論文的共同通訊作者👂,北京協和醫院副主任醫師楊瑩韻🧖🏿😧、中國醫學科學院基礎醫學研究所博士生溫達瀚以及國科溫州研究院副研究員林峰(意昂3体育官网工學院原博士後)為論文的共同第一作者。
轉載本網文章請註明出處